您现在的位置是:懒洋洋新闻网 > 科技 >
福鹏程:艾伯维将继续投资中国市场加速新药和新适应症引入
科技 人已围观
简介近年来,随着中国审评审批制度改革的不断深化,患者对于全球创新成果的可及性不断提速。……...
随着我国社会老龄化进程的加速,巨大的未被满足的医疗需求,推动了创新药的高速发展,让中国成为全球医药研发的新高地,也让中国医药市场进入了一个新的发展阶段,坚定了跨国企业持续加码中国、深耕中国的信心。
“中国致力于创造一个鼓励创新的环境,包括完善的监管框架和知识产权保护。继续这一战略,中国将吸引众多跨国制药公司探索为中国患者提供创新的机会。”近日,艾伯维洲际区域高级副总裁福鹏程(Pierre-Claude Fumoleau)在接受记者采访时表示,创新是引领发展的“第一推动力”,艾伯维在十年内就能够跻身世界领先的制药公司行列,主要归功于其对创新的关注。

福鹏程在艾伯维“中国合作日”活动上致辞
多领域创新药物引入中国市场惠及广大患者
福鹏程介绍,作为一家全球领先的生物制药公司,艾伯维致力于为中国患者提供支持,并尽早将其一流的创新药物带到中国。自2013年以来,艾伯维在中国市场的产品数量已由5个扩增至逾20个,涵盖免疫学、肿瘤学、眼科学、神经科学和美学等多个领域。
在免疫学领域,艾伯维拥有修美乐(阿达木单抗)和瑞福(乌帕替尼)、Skyrizi(利生奇珠单抗)等创新药。在中国,瑞福(乌帕替尼)已先后获批7个适应症,其中5个被纳入国家医保目录。福鹏程介绍,接下来公司将着力保证瑞福(乌帕替尼)同步参加全球多个Ⅲ期临床研究,并且在后续能够实现中国与全球同步获批上市。
在肿瘤学领域,艾伯维的唯可来(维奈克拉)打破了中国急性髓系白血病(AML)治疗领域近几十年无突破性创新疗法的僵局,将中国AML治疗带入了靶向治疗时代。该产品已于2023年进入国家医保,是目前AML领域唯一纳入医保的靶向药物,极大地降低了患者的负担。
青光眼引流管赞宜是中国首个使用真实世界证据辅助临床评价获批的青光眼微创引流管。
福鹏程透露,中国目前积极参与了艾伯维85%的全球多中心三期临床试验,目前有90多项是正在进行和计划中的临床试验。艾伯维计划到2030年在中国市场推出40多种新产品和适应症。“通过提供创新的解决方案和先进的药物,帮助医生不断完善治疗计划,并为中国患者提供支持,我们旨在为‘健康中国2030’做出贡献,并成为中国市场增长的重要推动力量。”福鹏程表示。
持续加码中国市场积极推进创新产品管线
近年来,随着中国审评审批制度改革的不断深化,患者对于全球创新成果的可及性不断提速。
“中国监管部门提出优化创新药物的审评审批机制,加快新药和优质药物的上市速度。这使得许多创新药物在获批当年即进入医保目录,大大提高了创新药物的可及性。”福鹏程介绍,艾伯维在免疫学领域的创新药物瑞福和用于治疗急性髓系白血病的靶向药物唯可来,几乎与美国、欧洲等市场实现同步批准和上市,并被纳入中国国家医保目录,提高了中国患者对关键药物的可及性。
作为全球第二大医药市场,中国巨大的市场规模和增长潜力,让跨国药企越来越重视中国市场,而中国本土的医药创新势力也在加速融入世界。
“随着国内生物技术行业的发展和每年越来越多的医疗创新来自中国,中国政府更加致力于为创新型企业建立一个生态系统,无论它们是本土企业还是跨国公司。”福鹏程表示,作为制药企业,艾伯维会根据不断发展的营商环境来制定投资策略。艾伯维期待与中国相关产业链、资本链、创新链等更多潜在伙伴加深合作、携手向前,不断推出创新疗法,加速推动中国创新药物和医疗行业在全球发展。
据悉,9月18日,艾伯维“中国合作日”首次线下活动在上海举行。此前,艾伯维“中国合作日”活动已连续举办三届线上活动。艾伯维希望借助“中国合作日”寻找在中国等亚太区域国家(地区)的创新型生物企业,探索跨境合作新机遇。
“艾伯维将继续在中国市场进行投资,推动免疫学、肿瘤学和眼科等核心产品的增长,积极推进创新产品管线,加速新药和新适应症的引入,提高治疗标准,扩大患者的用药可及性,以满足未被满足的医疗需求。”福鹏程说。(完)
相关文章
随机图文

激光显示“向新”!150吋海信激光电视即
9月19日,2024激光显示技术与产业发展大会在青岛举行。…………
北投台湖产业园二期举办招商推介会
加快建设数据基础制度综合改革试验田和数据要素集聚区,为北京数字经济发展持续贡献力量。…………
中国科技馆与中国防痨协会联合举办全国科普
“提升科学素养,共享健康生活”…………
2024年全国科普日广西活动暨八桂科普大
2024年全国科普日广西活动暨八桂科普大行动启动 9月19日,以“提升全民科学素质,协力建设科技强国”为主题的2024年...……
2024服贸会| 浪潮云洲获评业态创新服
9月12日至16日,2024年中国国际服务贸易交易会(简称“服贸会”)在北京举行。…………
福鹏程:艾伯维将继续投资中国市场加速新药
近年来,随着中国审评审批制度改革的不断深化,患者对于全球创新成果的可及性不断提速。…………
免疫记忆——清华大学医学院终身教授祁海团
认真走好脚下的路,远方的田野终有到达的时候。…………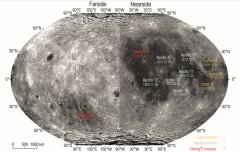
填补月背研究历史空白,嫦娥六号月球样品成
记者18日从中国科学院国家天文台获悉,我国科学家揭秘了嫦娥六号月球样品的物理、矿物和地球化学特征,解析了其中蕴含的月球早...……